ایرانیان تحلیل-انتشار نتایج یک پژوهش مشترک از دانشگاههای واشینگتن و نورثوسترن، موج جدیدی از امید را در حوزه درمان تومورهای مرگبار مغز ایجاد کرده است. این مطالعه نشان میدهد که میتوان با چند قطره داروی بینی و بهرهگیری از اعصاب صورت، نانوداروها را بدون جراحی به مغز رساند و تومورهای سختدرمانی مانند گلیوبلاستوما را در […]
ایرانیان تحلیل-انتشار نتایج یک پژوهش مشترک از دانشگاههای واشینگتن و نورثوسترن، موج جدیدی از امید را در حوزه درمان تومورهای مرگبار مغز ایجاد کرده است. این مطالعه نشان میدهد که میتوان با چند قطره داروی بینی و بهرهگیری از اعصاب صورت، نانوداروها را بدون جراحی به مغز رساند و تومورهای سختدرمانی مانند گلیوبلاستوما را در مدلهای حیوانی به طور کامل از بین برد. تحلیل حاضر ابعاد علمی، پیامدهای آینده و پرسشهای کلیدی این دستاورد را بررسی میکند.
بزرگترین مانع درمان: سد خونی–مغزی
جایگاه گلیوبلاستوما در میان مرگبارترین سرطانهای انسانی اتفاقی نیست. این تومور نهتنها رشد سریع دارد، بلکه پشت سدهای بیولوژیکی مغز پنهان میشود؛ سدهایی که برای محافظت ساخته شدهاند اما در عمل اجازه ورود داروهای ضدسرطان را نمیدهند. از دید متخصصان، همین سد چندلایه در بسیاری از موارد باعث میشود داروها حتی پیش از رسیدن به محل تومور از بین بروند.
در این شرایط، درمانهای رایج مانند جراحی، شیمیدرمانی یا تزریق مستقیم به مغز با خطرات و محدودیتهای جدی همراه است. به همین دلیل، تیم پژوهشی آمریکا رویکرد کاملاً متفاوتی را آزمایش کرده است: استفاده از مسیر عصبی طبیعی بدن.
ایدهای ساده با اثری شگفتآور: انتقال دارو از راه بینی
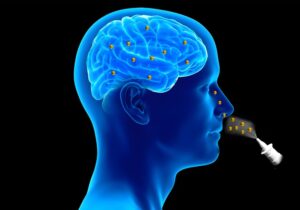
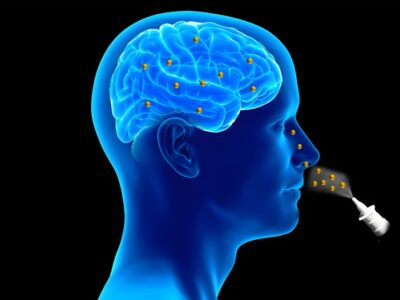
به گزارش ایرانیان تحلیل پژوهشگران نشان دادهاند که میتوان دارو را از طریق بینی و از مسیر عصب سهقلو و عصب بویایی به مغز رساند؛ مسیری که برخلاف جریان خون، مانعی ایجاد نمیکند.
نکته قابل توجه این است که دارو «درون حفره بینی باقی نمیماند» بلکه همانند یک پیام سریع عصبی، بهطور مستقیم وارد بافت مغز میشود. این کشف میتواند معادلات درمان سرطانهای مغزی را تغییر دهد، زیرا نیاز به جراحیهای پرخطر را کاهش میدهد و از مواجهه دارو با سایر اندامها جلوگیری میکند.
قلب فناوری: نانوساختارهای نوکلئیکاسیدی (SNA)
این موفقیت بر پایه طراحی ساختارهای نانویی خاصی به نام نوکلئیکاسیدهای کروی (SNA) بنا شده است؛ ذراتی با هسته طلا و پوشش متراکم DNA که مانند «کلیدهای مولکولی» رفتار میکنند. این پوشش DNA، هنگامیکه وارد سلولهای ایمنی مغز میشود، پیام هشدار ایجاد میکند.
از دید دانشمندان، این دقیقاً همان چیزی است که تومورهای «سرد» مانند گلیوبلاستوما نمیخواهند:
فعال شدن سیستم ایمنی.
تبدیل دشمن به مدافع؛ حمله ماکروفاژها به تومور
در حالت عادی، ماکروفاژهای اطراف گلیوبلاستوما در خدمت تومور هستند و با سرکوب ایمنی محلی، به بقای آن کمک میکنند.
اما SNAها این روند را تغییر میدهند:
-
DNA موجود روی ذرات به حسگر cGAS متصل میشود
-
سیستم ایمنی پیام ورود یک عامل بیگانه را دریافت میکند
-
مسیر STING فعال میشود
-
ماکروفاژها از «حالت حمایتی» به «حالت تهاجمی» تغییر میکنند
-
تومور هدف حمله گسترده قرار میگیرد
این فعالسازی بدون نیاز به تزریق مستقیم در بافت مغز انجام میشود؛ نقطهای که بسیاری از متخصصان آن را «تحولآفرین» توصیف میکنند
نتایج حیوانی: حذف کامل تومور و ایجاد حافظه ایمنی
یکی از نکات برجسته یافتهها، تأثیر دوگانه درمان است:
-
درمان تکعاملی:
قطره بینی به تنهایی اندازه تومور را بهطور معناداری کاهش داده است. -
درمان ترکیبی:
ترکیب آن با مهارکنندههای نقاط وارسی ایمنی موجب حذف کامل تومور در مدلهای حیوانی شده است.
این پایان کار نیست؛ پژوهشها نشان میدهد حیوانات پس از درمان، حافظه ایمنی پایدار کسب میکنند و در مواجهه دوباره با سلولهای تومور، از بازگشت بیماری جلوگیری میکنند. این یافته، امکان توسعه درمانهای بلندمدت و قابل پیشگیری را مطرح میکند.
یک پلتفرم قابل توسعه با کارکردهای چندگانه
الکساندر استگ، نویسنده همکار مطالعه، تأکید دارد که SNA تنها یک نانودارو نیست؛ بلکه «یک پلتفرم» است.
ماهیت مدولار این ساختار اجازه میدهد توالیهای DNA بسته به نوع تومور تغییر کنند.
به بیان دیگر:
چند قطره بینی میتواند در آینده حامل ترکیبی از فعالکنندههای ایمنی، هدفگیرهای ژنتیکی و مهارکنندههای مولکولی باشد.
چنین ترکیبی میتواند همزمان چند مسیر اصلی رشد سرطان را مسدود کند؛ رویکردی که متخصصان آن را مرحله بعدی درمانهای هوشمند میدانند
دیدگاههای انتقادی: چه چالشهایی باقی مانده است؟
با وجود موفقیتهای گسترده، چند سؤال مهم مطرح است:
۱. انتقال یافتهها به انسان چقدر زمان میبرد؟
سیستم عصبی انسان پیچیدهتر از مدلهای حیوانی است، بنابراین مراحل بالینی ممکن است زمانبر باشد.
۲. ایمنی نانوساختارها در استفاده بلندمدت چگونه ارزیابی میشود؟
وجود هسته طلا و تحریک شدید سیستم ایمنی نیازمند بررسیهای دقیق است.
۳. آیا همه تومورهای مغزی به این روش پاسخ میدهند؟
گلیوبلاستوما یک مدل «سرد» است، اما دیگر تومورها ممکن است رفتار متفاوتی داشته باشند.
پیامدهای گسترده برای درمانهای غیرتهاجمی
اگر این روش در انسان اثربخش باشد، مسیرهای جدیدی برای درمان سختترین بیماریهای مغز باز خواهد شد؛ از جمله:
-
تومورهای مقاوم درمان
-
اختلالات التهابی مغز
-
بیماریهای تحلیلبرنده عصبی
-
رساندن RNA و DNA درمانی بدون جراحی
برخی تحلیلگران حوزه پزشکی نیز این روش را «شروع موج جدیدی از ایمونوتراپیهای غیرتهاجمی» عصر نانو میدانند.
جمعبندی تحلیلی
پژوهش جدید منتشرشده در PNAS یک نقطه عطف در مبارزه با گلیوبلاستوما محسوب میشود. برای نخستینبار نشان داده شده است که:
-
میتوان سد خونی–مغزی را بدون آسیب دور زد
-
میتوان ایمونوتراپی را با چند قطره بینی وارد مغز کرد
-
میتوان تومورهای مرگبار را بدون جراحی هدف قرار داد
-
میتوان حافظه ایمنی پایدار ایجاد کرد
با وجود چالشهای پیشرو، این دستاورد نوید میدهد که آینده درمان سرطانهای مغزی ممکن است از مسیرهای سادهتر و کمتهاجمی عبور کند.
- نویسنده : ایرانیان تحلیل
- منبع خبر : ایرنا